|
Redacción. Madrid
La Agencia Española de Medicamentos (Aemps) ha tenido conocimiento a través de una denuncia de la comercialización de determinados productos (Escimax-t, T-sense y Sexcellence, de la empresa Terlex) que incluyen en su composición vardenafilo, sildenafilo, tadalafilo, 4-propoxi-N-hidroxietil-tiosildenafilo y desmetil-tiosildenafilo, sustancias farmacológicamente activas, lo cual les conferiría la consideración legal de medicamentos según lo establecido en el artículo 8 de la Ley 29/2006, de 26 de julio, de garantías y uso racional de los medicamentos y productos sanitarios.
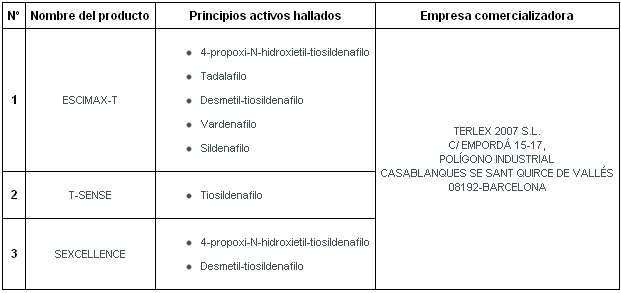
Análisis de la Agencia.
|
Estos productos se ofrecen en Internet como una alternativa de origen natural para mejorar las relaciones de pareja tanto para hombres como mujeres, indicando que se trata de una mezcla de plantas.
Este grupo de sustancias actúan restaurando la función eréctil deteriorada mediante el aumento del flujo sanguíneo del pene por inhibición selectiva de la fosfodiesterasa 5 (PDE5). Están contraindicados en pacientes con infarto agudo de miocardio, angina inestable, angina de esfuerzo, insuficiencia cardiaca, arritmias incontroladas, hipotensión o hipertensión arterial no controlada, ictus, y personas con antecedentes de neuropatía óptica isquémica anterior no arterítica.
Este grupo de principios activos presenta numerosas interacciones con otros medicamentos, pudiendo además aparecer reacciones adversas de diversa gravedad, a tener en consideración, como cardiovasculares, ya que su consumo se ha asociado a infarto agudo de miocardio, angina inestable, arritmia ventricular, palpitaciones, taquicardias, accidente cerebro vascular, incluso muerte súbita cardiaca, aunque en mayor medida se han presentado en pacientes con antecedentes de factores de riesgo cardiovascular. También pueden presentarse cefaleas, mareos, dispepsia, dolor abdominal, congestión nasal, mialgias, dolor de espalda, reacciones de hipersensibilidad como urticaria, erupciones exantemáticas, erupciones cutáneas y/o dermatitis, alteraciones oculares y visuales, etc.
Considerando lo anteriormente mencionado, así como que los citados productos no han sido objeto de evaluación y autorización previa a la comercialización por parte de la Agencia Española de Medicamentos y Productos Sanitarios, como consta en el Real Decreto 520/1999, de 26 de marzo, por el que se aprueba el Estatuto de la Agencia Española del Medicamento y el artículo 9.1 de la Ley 29/2006, de 26 de julio, siendo su presencia en el mercado ilegal, la Directora de la Agencia Española de Medicamentos y Productos Sanitarios conforme a lo establecido en el artículo 99 de la citada Ley y en relación con el mencionado Real Decreto, ha resuelto ordenar la retirada del mercado de todos los ejemplares de los citados productos.
|